
- Müəllif Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:33.
- Son dəyişdirildi 2025-01-22 16:55.
İdeal Qaz Qanunu, deyildiyi kimi, əslində belədir PV = nRT , bütün standart dəyişənlərlə. Burada n=m/M, burada m qazın kütləsi və M qazın molekulyar çəkisidir. Qısacası R in PV = nRT R-i almaq üçün afaktor M (molekulyar çəki) tərəfindən kiçildilir PV = mRT.
Sadəcə olaraq, pV nRT-də r nəyə bərabərdir?
İdeal qaz qanunu belədir: pV = nRT , burada n molların sayıdır və R universal qaz sabitidir. dəyəri R cəlb edilən vahidlərdən asılıdır, lakin adətən S. I. vahidləri ilə aşağıdakı kimi ifadə edilir: R = 8,314 J/mol. Bu o deməkdir ki, hava üçün dəyərdən istifadə edə bilərsiniz R = 287 J/kq.
Eynilə, kimya pV nRT-də R nə deməkdir? Universal qaz sabitinin vahidləri R PV=n tənliyindən alınır R T. O dayanır Regnault üçün.
Bu baxımdan, pV nRT-də N nəyi ifadə edir?
. P (təzyiq) × V (həcm) = (molların sayı) × R (qaz sabiti) × T (Kelvində temperatur) olduğu ideal qazın ölçülə bilən xassələrinin əlaqəsini təsvir edən fiziki qanun. Boyle, Charles və Avogadro qaz qanunlarının birləşməsindən əldə edilmişdir. Universal qaz qanunu da deyilir.
İdeal qaz qanununda M nədir?
Orijinal ideal qaz qanunu sıxlıq versiyası olan PV =nRT düsturundan istifadə edir ideal qaz qanunu PM = dRT, burada P atmosferdə (atm) ölçülən təzyiqdir, T kelvinlə (K) ölçülür, R isə ideal qaz qanunu sabit 0,0821 at m (L) m ol(K) ilkin düsturda olduğu kimi, lakin M indi molar kütlədir (g m ol
Tövsiyə:
Osmoz diffuziyası ilə asanlaşdırılmış diffuziya arasındakı fərq nədir?

Suyun bir hüceyrədən digərinə keçdiyi zaman da osmoz baş verir. Digər tərəfdən asanlaşdırılmış diffuziya hüceyrəni əhatə edən mühit hüceyrə daxilindəki mühitdən daha çox ion və ya molekul konsentrasiyasında olduqda baş verir. Molekullar diffuziya qradiyenti səbəbindən ətraf mühitdən hüceyrəyə keçir
Korrelyasiya ilə chi kvadratı arasındakı fərq nədir?
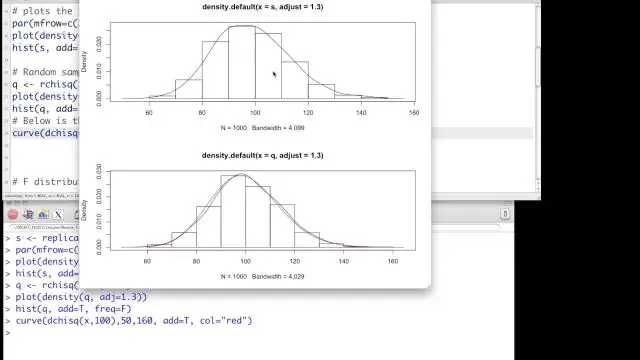
Beləliklə, korrelyasiya iki dəyişən arasındakı xətti əlaqə haqqındadır. Adətən, hər ikisi davamlıdır (və ya təxminən belədir), lakin birinin dixotom olduğu vəziyyət üçün dəyişikliklər var. Ki-kvadrat adətən iki dəyişənin müstəqilliyinə aiddir. Adətən, hər ikisi kateqoriyalıdır
İqlim zonası ilə biom arasındakı fərq nədir?

İqlim atmosfer istiliyinə və yağıntıya görə təsnif edilir, biom isə ilk növbədə vahid bitki örtüyünün növlərinə görə təsnif edilir. İqlim hansı biomun mövcud olduğunu müəyyən edə bilər, lakin bir biom adətən iqlimə eyni şəkildə nəzarət etmir və ya ona təsir etmir
Ümumi kimya ilə üzvi kimya arasındakı fərq nədir?
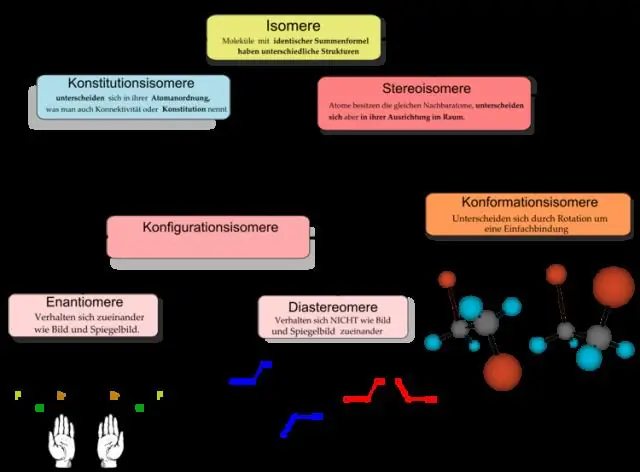
Üzvi kimya kimyanın alt bölməsi hesab olunur. Ümumi çətir termini "kimya" ümumiyyətlə bütün maddələrin tərkibi və çevrilmələri ilə əlaqəli olduğu halda, üzvi kimya yalnız üzvi birləşmələrin öyrənilməsi ilə məhdudlaşır
Sitoplazmik reaksiya ilə nüvə reaksiyası arasındakı fərq nədir?

Nüvə reaksiyası ilə sitoplazmik reaksiya arasındakı fərq nədir? Nüvə reaksiyası gen ifadəsinin dəyişdirilməsini, sitoplazmik reaksiya isə fermentin aktivləşməsini və ya ion kanalının açılmasını əhatə edir
